Ang
Thermodynamics ng gaseous aggregate state of matter ay isang mahalagang sangay ng physics na nag-aaral ng thermodynamic equilibrium at quasi-static transition sa mga system. Ang pangunahing modelo kung saan nakabatay ang mga hula ng pag-uugali ng mga system ay ang perpektong modelo ng gas. Sa paggamit nito, nakuha ang Mendeleev-Clapeyron equation. Isaalang-alang ito sa artikulo.
Ideal na gas
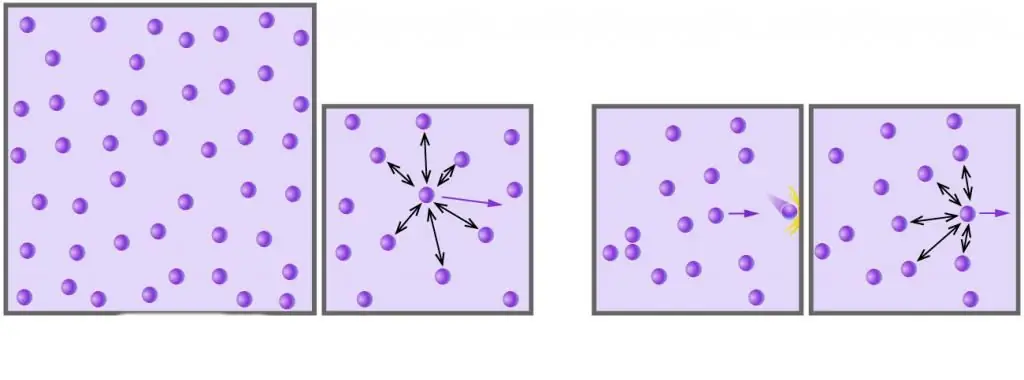
Tulad ng alam mo, ang lahat ng tunay na gas ay binubuo ng mga molekula o atomo, ang mga distansya sa pagitan nito ay masyadong malaki kumpara sa kanilang sukat sa mababang presyon. Bilang karagdagan, sa mataas na temperatura, sa isang ganap na sukat, ang kinetic energy ng mga molekula ay lumampas sa kanilang potensyal na enerhiya na nauugnay sa mahinang dipole-dipole na pakikipag-ugnayan (kung, bilang karagdagan sa mga pakikipag-ugnayang ito, mayroong iba pang mga uri ng mga bono ng kemikal, halimbawa, ionic o hydrogen, pagkatapos ay gumawa sila ng malaking kontribusyon sa potensyal na bahagi ng panloob na enerhiya ng system).
Dahil saPara sa maraming mga tunay na gas sa ilalim ng mga kondisyon na malapit sa normal, maaaring pabayaan ng isa ang kanilang panloob na pakikipag-ugnayan at laki ng butil. Binubuo ng dalawang pangunahing pagtatantya na ito ang perpektong modelo ng gas.
Equation ni Mendeleev sa physics

Mas tama at patas na tawagan ang equation na ito na batas ng Clapeyron-Mendeleev. Ang katotohanan ay una itong naitala ng inhinyero ng Pransya na si Emile Clapeyron noong 1834. Ginawa niya ito sa pamamagitan ng pagsusuri sa mga batas sa gas ng Boyle-Mariotte, Gay-Lussac at Charles na natuklasan sa simula ng ika-19 na siglo.
Ang merito ng Russian chemist na si Dmitry Mendeleev ay nakasalalay sa katotohanan na binigyan niya ang equation ng moderno at madaling gamitin na mathematical form. Sa partikular, ipinakilala ni Mendeleev sa equation ang isang pare-pareho para sa lahat ng mga gas R=8, 314 J/(molK). Si Clapeyron mismo ay gumamit ng ilang empirical constants na nagpapahirap sa proseso ng computational.
Ang equation ng Mendeleev-Clapeyron ay nakasulat tulad ng sumusunod:
PV=nRT.
Ang pagkakapantay-pantay na ito ay nangangahulugan na ang produkto ng pressure P at volume V sa kaliwang bahagi ng expression ay palaging proporsyonal sa produkto ng ganap na temperatura T at ang dami ng substance n sa kaliwang bahagi.
Ang expression na pinag-aaralan ay nagbibigay-daan sa iyong makakuha ng anumang batas sa gas kung aayusin mo ang dalawa sa apat na parameter nito. Sa kaso ng isoprocesses, ang mga closed system ay pinag-aaralan kung saan walang palitan ng matter sa kapaligiran (n=const). Ang mga prosesong ito ay nailalarawan sa pamamagitan ng isang nakapirming thermodynamic parameter (T, P o V).

Halimbawang problema
Ngayon, lutasin natin ang problema sa Mendeleev-Clapeyron equation. Ito ay kilala na ang oxygen na tumitimbang ng 500 gramo ay nasa isang silindro na may dami ng 100 litro sa isang presyon ng 2 atmospheres. Ano ang temperatura sa balloon, dahil nasa thermodynamic equilibrium ang system.
Tandaan na, ayon sa kahulugan, ang dami ng isang substance ay kinakalkula ng formula:
n=m/M.
Kung saan ang m ay ang masa ng lahat ng mga particle ng system, ang M ay ang kanilang average na molar mass. Ang pagkakapantay-pantay na ito ay nagpapahintulot sa amin na muling isulat ang Mendeleev equation sa sumusunod na anyo:
PV=mRT/M.
Kung saan natin nakukuha ang gumaganang formula para sa gawaing ito:
T=PVM/(mR).
Nananatili itong i-convert ang lahat ng dami sa mga unit ng SI at palitan ang mga ito sa expression na ito:
T=21013250, 10, 032/(0, 58, 314)=156 K.
Ang kinakalkula na temperatura ay -117 oC. Bagama't gaseous pa rin ang oxygen sa temperaturang ito (namumuo ito sa -182.96 oC), sa ilalim ng gayong mga kundisyon, magagamit lamang ang ideal na modelo ng gas upang makakuha ng qualitative estimate ng kinakalkulang halaga.






