Ang kaalaman sa mga kahulugan sa physics ay isang pangunahing salik para sa matagumpay na paglutas ng iba't ibang pisikal na problema. Sa artikulo, isasaalang-alang natin kung ano ang ibig sabihin ng isobaric, isochoric, isothermal at adiabatic na proseso para sa isang perpektong sistema ng gas.
Ideal na gas at ang equation nito
Bago magpatuloy sa paglalarawan ng isobaric, isochoric at isothermal na proseso, isaalang-alang natin kung ano ang ideal na gas. Sa ilalim ng kahulugang ito sa physics, isinasaalang-alang nila ang isang sistema na binubuo ng isang malaking bilang ng mga walang sukat at hindi nakikipag-ugnayan na mga particle na gumagalaw sa mataas na bilis sa lahat ng direksyon. Sa katunayan, pinag-uusapan natin ang tungkol sa isang gas na pinagsama-samang estado ng bagay, kung saan ang mga distansya sa pagitan ng mga atom at molekula ay higit na lumalampas sa kanilang mga sukat at kung saan ang potensyal na enerhiya ng pakikipag-ugnayan ng mga particle ay napapabayaan dahil sa liit nito, kumpara sa kinetic energy.
Ang estado ng ideal na gas ay ang kabuuan ng mga thermodynamic na parameter nito. Ang mga pangunahing ay temperatura, dami at presyon. Tukuyin natin ang mga ito sa pamamagitan ng mga letrang T, V at P, ayon sa pagkakabanggit. Sa 30s ng XIX na sigloSi Clapeyron (isang French scientist) ay unang nagsulat ng isang equation na pinagsasama ang mga ipinahiwatig na thermodynamic parameter sa loob ng iisang pagkakapantay-pantay. Mukhang:
PV=nRT,
kung saan ang n at R ay ang dami ng mga sangkap at ang gas constant, ayon sa pagkakabanggit.
Ano ang isoprocesses sa mga gas?
Tulad ng napansin ng marami, ang isobaric, isochoric at isothermal na proseso ay gumagamit ng parehong prefix na "iso" sa kanilang mga pangalan. Nangangahulugan ito ng pagkakapantay-pantay ng isang thermodynamic parameter sa panahon ng pagpasa ng buong proseso, habang nagbabago ang natitirang mga parameter. Halimbawa, ang isang isothermal na proseso ay nagpapahiwatig na, bilang resulta, ang ganap na temperatura ng system ay pinananatiling pare-pareho, habang ang isang isochoric na proseso ay nagpapahiwatig ng isang pare-parehong volume.
Ang
Isoprocesses ay maginhawang pag-aralan, dahil ang pag-aayos ng isa sa mga thermodynamic na parameter ay humahantong sa pagpapasimple ng pangkalahatang equation ng estado ng gas. Mahalagang tandaan na ang mga batas ng gas para sa lahat ng mga isoprocess na ito ay natuklasan nang eksperimento. Ang kanilang pagsusuri ay nagbigay-daan kay Clapeyron na makuha ang pinababang unibersal na equation.
Isobaric, isochoric at isothermal na proseso
Natuklasan ang unang batas para sa isang isothermal na proseso sa isang ideal na gas. Ngayon ito ay tinatawag na batas ng Boyle-Mariotte. Dahil ang T ay hindi nagbabago, ang equation ng estado ay nagpapahiwatig ng pagkakapantay-pantay:
PV=const.
Sa madaling salita, ang anumang pagbabago sa presyon sa system ay humahantong sa isang inversely proportional na pagbabago sa volume nito, kung ang temperatura ng gas ay pinananatiling pare-pareho. Ang graph ng function na P(V) ayhyperbole.
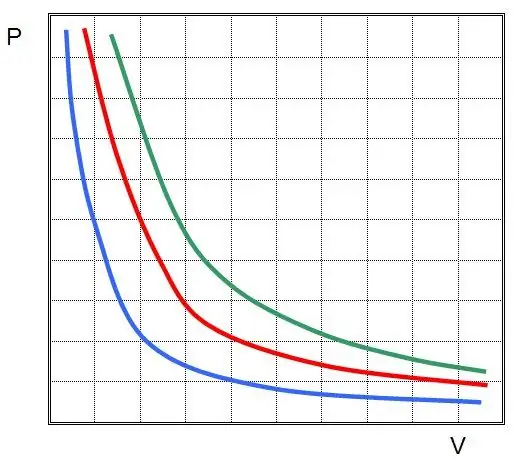
Isobaric na proseso - ito ay isang pagbabago sa estado ng system, kung saan ang presyon ay nananatiling pare-pareho. Kapag naayos na ang halaga ng P sa Clapeyron equation, nakuha natin ang sumusunod na batas:
V/T=const.
Ang pagkakapantay-pantay na ito ay may pangalan ng French physicist na si Jacques Charles, na tumanggap nito sa pagtatapos ng ika-18 siglo. Ang isobar (graphic na representasyon ng V(T) function) ay mukhang isang tuwid na linya. Kung mas maraming pressure sa system, mas mabilis na tumataas ang linyang ito.
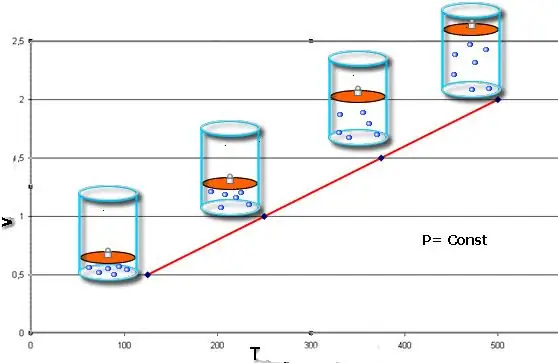
Ang isobaric na proseso ay madaling ipatupad kung ang gas ay pinainit sa ilalim ng piston. Ang mga molekula ng huli ay nagpapataas ng kanilang bilis (kinetic energy), lumilikha ng mas mataas na presyon sa piston, na humahantong sa pagpapalawak ng gas at pagpapanatili ng pare-parehong halaga ng P.
Sa wakas, ang ikatlong isoprocess ay isochoric. Ito ay tumatakbo nang may pare-parehong volume. Mula sa equation ng estado ay nakukuha natin ang katumbas na pagkakapantay-pantay:
P/T=const.
Kilala ito sa mga physicist bilang batas ni Gay-Lussac. Ang direktang proporsyonalidad sa pagitan ng presyon at ganap na temperatura ay nagpapahiwatig na ang graph ng isochoric na proseso, tulad ng graph ng isobaric, ay isang tuwid na linya na may positibong slope.
Mahalagang maunawaan na ang lahat ng isoprocess ay nagaganap sa mga closed system, ibig sabihin, ang halaga ng n ay pinapanatili sa panahon ng kanilang kurso.
Adiabatic na proseso
Ang prosesong ito ay hindi kabilang sa kategoryang "iso", dahil nagbabago ang lahat ng tatlong thermodynamic na parameter sa panahon ng pagpasa nito. adiabatictinatawag na transisyon sa pagitan ng dalawang estado ng sistema, kung saan hindi ito nakikipagpalitan ng init sa kapaligiran. Kaya, ang pagpapalawak ng system ay isinasagawa dahil sa mga panloob na reserbang enerhiya nito, na humahantong sa isang makabuluhang pagbaba sa presyon at ganap na temperatura sa loob nito.
Adiabatic na proseso para sa isang perpektong gas ay inilalarawan ng mga equation ni Poisson. Ang isa sa mga ito ay ipinapakita sa ibaba:
PVγ=const,
kung saan ang γ ay ang ratio ng mga kapasidad ng init sa pare-parehong presyon at sa pare-parehong volume.
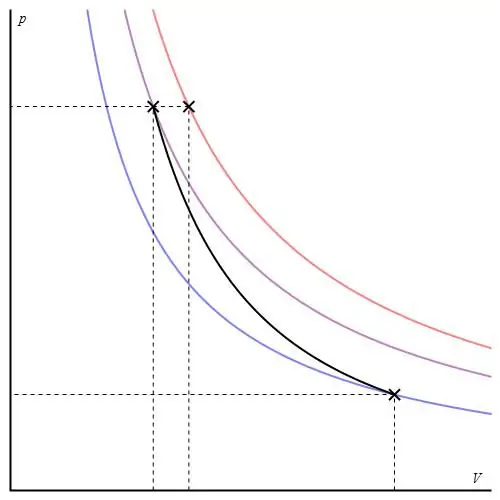
Ang adiabatic graph ay naiiba sa isochoric process graph at sa isobaric graph, ngunit ito ay katulad ng isang hyperbola (isotherm). Ang adiabat sa P-V axes ay kumikilos nang mas matindi kaysa sa isotherm.






