Isa sa mga mahahalagang tanong sa pag-aaral ng mga thermodynamic system sa pisika ay ang tanong kung ang sistemang ito ay makakagawa ng ilang kapaki-pakinabang na gawain. Ang malapit na nauugnay sa konsepto ng trabaho ay ang konsepto ng panloob na enerhiya. Sa artikulong ito, isasaalang-alang natin kung ano ang panloob na enerhiya ng isang ideal na gas at magbibigay ng mga formula para sa pagkalkula nito.
Ideal na gas
Tungkol sa gas, bilang isang estado ng pagsasama-sama, na walang anumang nababanat na puwersa sa ilalim ng panlabas na impluwensya dito at, bilang isang resulta, ay hindi nagpapanatili ng dami at hugis, alam ng bawat mag-aaral. Ang konsepto ng isang perpektong gas para sa marami ay nananatiling hindi maintindihan at hindi malinaw. Ipaliwanag natin.
Ang ideal na gas ay anumang gas na nakakatugon sa sumusunod na dalawang mahalagang kundisyon:
- Walang sukat ang mga particle na bumubuo dito. May sukat nga ang mga ito, ngunit napakaliit nito kumpara sa mga distansya sa pagitan nila na maaari itong balewalain sa lahat ng mathematical calculations.
- Ang mga particle ay hindi nakikipag-ugnayan sa isa't isa gamit ang mga puwersa o puwersa ng van der Waalsibang kalikasan. Sa katunayan, sa lahat ng totoong gas, naroroon ang gayong pakikipag-ugnayan, ngunit ang enerhiya nito ay bale-wala kumpara sa average na enerhiya ng mga kinetic particle.
Ang inilarawan na mga kondisyon ay natutugunan ng halos lahat ng mga tunay na gas, ang temperatura nito ay higit sa 300 K, at ang mga presyon ay hindi lalampas sa isang kapaligiran. Para sa masyadong mataas na presyon at mababang temperatura ay sinusunod ang paglihis ng mga gas mula sa perpektong pag-uugali. Sa kasong ito, ang isa ay nagsasalita ng mga tunay na gas. Inilalarawan ang mga ito ng van der Waals equation.
Ang konsepto ng panloob na enerhiya ng isang perpektong gas
Alinsunod sa kahulugan, ang panloob na enerhiya ng isang sistema ay ang kabuuan ng kinetic at potensyal na enerhiya na nasa loob ng sistemang ito. Kung ang konseptong ito ay inilapat sa isang perpektong gas, kung gayon ang potensyal na sangkap ay dapat na itapon. Sa katunayan, dahil ang mga particle ng isang perpektong gas ay hindi nakikipag-ugnayan sa isa't isa, maaari silang ituring na malayang gumagalaw sa ganap na vacuum. Upang kunin ang isang particle mula sa system na pinag-aaralan, hindi kailangang gumawa ng trabaho laban sa mga panloob na puwersa ng pakikipag-ugnayan, dahil ang mga puwersang ito ay wala.
Kaya, ang panloob na enerhiya ng isang perpektong gas ay palaging kasabay ng kinetic energy nito. Ang huli, sa turn, ay natatanging tinutukoy ng molar mass ng mga particle ng system, ang kanilang numero, pati na rin ang average na bilis ng translational at rotational motion. Ang bilis ng paggalaw ay depende sa temperatura. Ang pagtaas ng temperatura ay humahantong sa pagtaas ng panloob na enerhiya, at kabaliktaran.
Formula para sapanloob na enerhiya
Ipahiwatig ang panloob na enerhiya ng isang perpektong sistema ng gas na may letrang U. Ayon sa thermodynamics, tinukoy ito bilang pagkakaiba sa pagitan ng enthalpy H ng system at ng produkto ng presyon at volume, iyon ay:
U=H - pV.
Sa talata sa itaas, nalaman namin na ang halaga ng U ay tumutugma sa kabuuang kinetic energy Ekng lahat ng gas particle:
U=Ek.
Mula sa statistical mechanics, sa loob ng framework ng molecular kinetic theory (MKT) ng isang ideal na gas, sumusunod na ang average na kinetic energy ng isang particle Ek1 ay katumbas ng sumusunod na halaga:
Ek1=z/2kBT.
Dito kB at T - Boltzmann constant at temperatura, z - bilang ng mga antas ng kalayaan. Ang kabuuang kinetic energy ng system Ek ay maaaring makuha sa pamamagitan ng pagpaparami ng Ek1 sa bilang ng mga particle N sa system:
Ek=NEk1=z/2NkBT.
Kaya, nakuha namin ang formula para sa panloob na enerhiya ng isang perpektong gas, na nakasulat sa pangkalahatang anyo sa mga tuntunin ng ganap na temperatura at bilang ng mga particle sa isang closed system:
U=z/2NkBT.
Monatomic at polyatomic gas
Ang formula para sa U na nakasulat sa nakaraang talata ng artikulo ay hindi maginhawa para sa praktikal na paggamit nito, dahil mahirap matukoy ang bilang ng mga particle N. Gayunpaman, kung isasaalang-alang natin ang kahulugan ng dami ng substance n, maaaring muling isulat ang expression na ito sa isang mas madaling paraan:
n=N/NA; R=NAkB=8, 314 J/(molK);
U=z/2nR T.
Ang bilang ng mga degree ng kalayaan z ay depende sa geometry ng mga particle na bumubuo sa gas. Kaya, para sa isang monoatomic gas, z=3, dahil ang isang atom ay maaaring gumalaw nang nakapag-iisa lamang sa tatlong direksyon ng espasyo. Kung ang gas ay diatomic, kung gayon ang z=5, dahil dalawa pang rotational degrees ng kalayaan ang idinaragdag sa tatlong translational degrees ng kalayaan. Panghuli, para sa anumang iba pang polyatomic gas, z=6 (3 translational at 3 rotational degrees of freedom). Sa pag-iisip na ito, maaari nating isulat sa sumusunod na anyo ang mga formula para sa panloob na enerhiya ng isang perpektong gas ng monatomic, diatomic at polyatomic:
U1=3/2nRT;
U2=5/2nRT;
U≧3=3nRT.
Halimbawa ng gawain upang matukoy ang panloob na enerhiya
Ang isang 100-litro na silindro ay naglalaman ng purong hydrogen sa presyon ng 3 atmospheres. Ipagpalagay na ang hydrogen ay isang perpektong gas sa ilalim ng mga partikular na kondisyon, kinakailangan upang matukoy kung ano ang panloob na enerhiya nito.

Ang mga formula sa itaas para sa U ay naglalaman ng dami ng substance at temperatura ng gas. Sa kondisyon ng problema, ganap na walang sinabi tungkol sa mga dami na ito. Upang malutas ang problema, kinakailangang alalahanin ang unibersal na Clapeyron-Mendeleev equation. Ito ay may hitsura na ipinapakita sa figure.
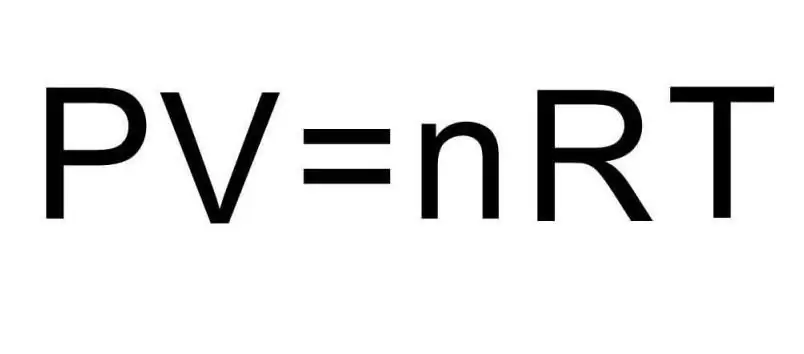
Dahil ang hydrogen H2 ay isang diatomic molecule, ang formula para sa internal energy ay:
UH2=5/2nRT.
Paghahambing ng parehong expression, dumating tayo sa panghuling formula para sa paglutas ng problema:
UH2=5/2PV.
Nananatili itong i-convert ang mga yunit ng presyon at volume mula sa kundisyon patungo sa SI system ng mga yunit, palitan ang kaukulang mga halaga sa formula para sa UH2at makuha ang sagot: UH2 ≈ 76 kJ.






