Ang kapasidad ng init ng isang gas ay ang dami ng enerhiya na sinisipsip ng katawan kapag pinainit ito ng isang degree. Suriin natin ang mga pangunahing katangian ng pisikal na dami na ito.

Mga Depinisyon
Ang tiyak na init ng isang gas ay ang unit mass ng isang partikular na substance. Ang mga yunit ng pagsukat nito ay J/(kg·K). Ang dami ng init na nasisipsip ng katawan sa proseso ng pagbabago ng estado ng pagsasama-sama nito ay nauugnay hindi lamang sa una at huling estado, kundi pati na rin sa paraan ng paglipat.

Department
Ang kapasidad ng init ng mga gas ay nahahati sa halagang tinutukoy sa pare-parehong volume (Cv), pare-parehong presyon (Cр).
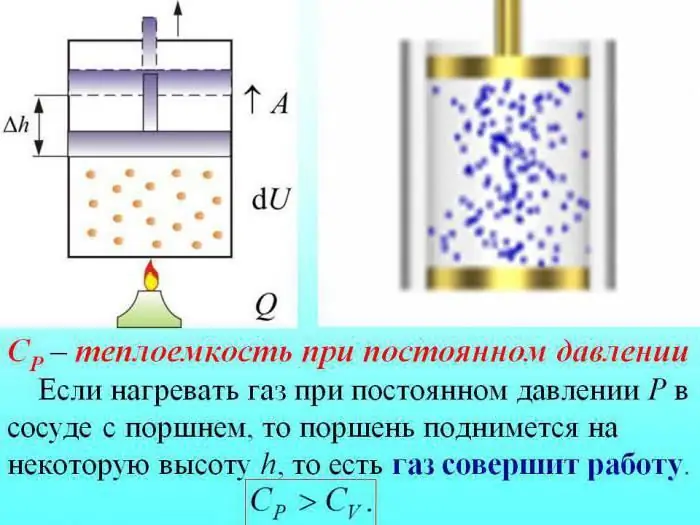
Sa kaso ng pag-init nang hindi binabago ang presyon, ang ilang init ay ginugugol upang makagawa ng gawain ng pagpapalawak ng gas, at ang bahagi ng enerhiya ay ginugugol upang mapataas ang panloob na enerhiya.
Ang kapasidad ng init ng mga gas sa pare-parehong presyon ay tinutukoy ng dami ng init na ginugugol sa pagtaas ng panloob na enerhiya.
Gas state: mga feature, paglalarawan
Ang kapasidad ng init ng isang ideal na gas ay tinutukoy na isinasaalang-alang ang katotohanan na Сp-Сv=R. Ang huling dami ay tinatawag na universal gas constant. Ang halaga nito ay tumutugma sa 8.314 J/(mol K).
Kapag nagsasagawa ng mga teoretikal na kalkulasyon ng kapasidad ng init, halimbawa, na naglalarawan ng kaugnayan sa temperatura, hindi sapat na gumamit lamang ng mga thermodynamic na pamamaraan, mahalagang armasan ang iyong sarili ng mga elemento ng static na pisika.
Ang kapasidad ng init ng mga gas ay nagsasangkot ng pagkalkula ng average na halaga ng enerhiya ng paggalaw ng pagsasalin ng ilang molekula. Ang nasabing paggalaw ay buod mula sa rotational at translational motion ng molekula, gayundin mula sa panloob na vibrations ng atoms.
Sa static physics, mayroong impormasyon na para sa bawat antas ng kalayaan ng rotational at translational motion, mayroong isang dami para sa isang gas na katumbas ng kalahati ng universal gas constant.

Mga kawili-wiling katotohanan
Ang isang particle ng isang monatomic gas ay ipinapalagay na mayroong tatlong translational degrees ng kalayaan, kaya ang partikular na init ng isang gas ay may tatlong translational, dalawang rotational, at isang vibrational degrees ng kalayaan. Ang batas ng kanilang pare-parehong pamamahagi ay humahantong sa equating ang tiyak na init sa isang pare-parehong volume sa R.
Sa panahon ng mga eksperimento, natagpuan na ang kapasidad ng init ng isang diatomic gas ay tumutugma sa halagang R. Ang gayong pagkakaiba sa pagitan ng teorya at kasanayan ay ipinaliwanag sa pamamagitan ng katotohanan na ang kapasidad ng init ng isang perpektong gas ay nauugnay sa quantum epekto, samakatuwid, kapag gumagawa ng mga kalkulasyon, mahalagang gumamit ng mga istatistika batay sa quantummekanika.
Batay sa mga pundasyon ng quantum mechanics, anumang sistema ng mga particle na nag-o-oscillate o umiikot, kabilang ang mga molekula ng gas, ay mayroon lamang ilang discrete values ng enerhiya.
Kung ang enerhiya ng thermal motion sa system ay hindi sapat upang pukawin ang mga oscillations ng isang partikular na frequency, ang mga naturang paggalaw ay hindi nakakatulong sa kabuuang kapasidad ng init ng system.
Bilang resulta, ang isang partikular na antas ng kalayaan ay nagiging "nagyeyelo", imposibleng ilapat ang batas ng equipartition dito.
Ang kapasidad ng init ng mga gas ay isang mahalagang katangian ng estado kung saan nakasalalay ang paggana ng buong thermodynamic system.
Ang temperatura kung saan maaaring ilapat ang batas ng equipartition sa vibrational o rotational degree of freedom ay nailalarawan ng quantum theory, nag-uugnay sa Planck constant sa Boltzmann constant.

Diatomic gases
Ang mga puwang sa pagitan ng mga antas ng paikot na enerhiya ng naturang mga gas ay isang maliit na bilang ng mga degree. Ang exception ay hydrogen, kung saan ang halaga ng temperatura ay tinutukoy ng daan-daang degrees.
Iyon ang dahilan kung bakit ang kapasidad ng init ng isang gas sa pare-parehong presyon ay mahirap ilarawan ng batas ng pare-parehong pamamahagi. Sa quantum statistics, kapag tinutukoy ang heat capacity, isinasaalang-alang na ang vibrational part nito, sa kaso ng pagbaba ng temperatura, ay mabilis na bumababa at umabot sa zero.
Ang hindi pangkaraniwang bagay na ito ay nagpapaliwanag sa katotohanan na sa temperatura ng silid ay halos walang vibrational na bahagi ng kapasidad ng init, para sadiatomic gas, tumutugma ito sa pare-parehong R.
Ang kapasidad ng init ng isang gas sa pare-parehong volume sa kaso ng mababang temperatura na mga indicator ay tinutukoy gamit ang quantum statistics. Mayroong prinsipyo ng Nernst, na tinatawag na ikatlong batas ng thermodynamics. Batay sa formulation nito, bababa ang molar heat capacity ng isang gas kasabay ng pagbaba ng temperatura, na nagiging zero.

Mga tampok ng solids
Kung ang kapasidad ng init ng isang pinaghalong gas ay maipaliwanag gamit ang mga istatistika ng quantum, kung gayon para sa isang solidong estado ng pagsasama-sama, ang thermal motion ay nailalarawan sa pamamagitan ng bahagyang pagbabagu-bago ng mga particle na malapit sa posisyon ng equilibrium.
Ang bawat atom ay may tatlong vibrational degrees ng kalayaan, samakatuwid, alinsunod sa equipartition law, ang molar heat capacity ng isang solid ay maaaring kalkulahin bilang 3nR, na ang n bilang ang bilang ng mga atom sa isang molekula.
Sa pagsasagawa, ang numerong ito ay ang limitasyon na maaaring maabot ng kapasidad ng init ng isang solidong katawan sa mataas na temperatura.
Maximum ay maaaring makuha sa ordinaryong temperatura para sa ilang elemento, kabilang ang mga metal. Para sa n=1, ang batas ng Dulong at Petit ay natutupad, ngunit para sa mga kumplikadong sangkap ay medyo mahirap maabot ang gayong limitasyon. Dahil hindi talaga makukuha ang limitasyon, nangyayari ang pagkabulok o pagkatunaw ng solid.
Kasaysayan ng quantum theory
Ang mga nagtatag ng quantum theory ay sina Einstein at Debye sa simula ng ikadalawampu siglo. Ito ay batay sa quantization ng oscillatory motions ng atoms sa isang tiyakkristal. Sa kaso ng mga tagapagpahiwatig ng mababang temperatura, ang kapasidad ng init ng isang solidong katawan ay lumalabas na direktang proporsyonal sa ganap na halaga na kinuha sa cubed. Ang relasyong ito ay tinawag na batas ni Debye. Bilang criterion na ginagawang posible na makilala ang mababa at mataas na mga indicator ng temperatura, ang kanilang paghahambing sa temperatura ng Debye ay kinuha.
Ang halagang ito ay tinutukoy ng spectrum ng mga vibrations ng isang atom sa katawan, samakatuwid ito ay seryosong nakasalalay sa mga katangian ng kristal na istraktura nito.
Ang
QD ay isang value na may ilang daang K, ngunit, halimbawa, mas mataas ito sa brilyante.
Ang mga conduction electron ay may malaking kontribusyon sa kapasidad ng init ng mga metal. Upang kalkulahin ito, ginagamit ang mga istatistika ng Fermi quantum. Ang electronic conductivity para sa mga metal na atom ay direktang proporsyonal sa ganap na temperatura. Dahil ito ay isang hindi gaanong halaga, ito ay isinasaalang-alang lamang sa mga temperatura na may posibilidad na ganap na zero.
Mga paraan para sa pagtukoy ng kapasidad ng init
Ang pangunahing pang-eksperimentong paraan ay calorimetry. Upang magsagawa ng teoretikal na pagkalkula ng kapasidad ng init, ginagamit ang statistical thermodynamics. Ito ay wasto para sa isang perpektong gas, gayundin para sa mga mala-kristal na katawan, ay isinasagawa batay sa pang-eksperimentong data sa istruktura ng bagay.
Ang mga empirikal na pamamaraan para sa pagkalkula ng kapasidad ng init ng isang perpektong gas ay batay sa ideya ng istrukturang kemikal, ang kontribusyon ng mga indibidwal na grupo ng mga atom sa Ср.
Para sa mga likido, ginagamit din ang mga pamamaraan na batay sa paggamit ng thermodynamicmga cycle na ginagawang posible na lumipat mula sa kapasidad ng init ng isang ideal na gas patungo sa isang likido sa pamamagitan ng derivative ng temperatura ng enthalpy ng proseso ng evaporation.
Sa kaso ng isang solusyon, ang pagkalkula ng kapasidad ng init bilang isang additive function ay hindi pinapayagan, dahil ang labis na halaga ng kapasidad ng init ng solusyon ay karaniwang makabuluhan.
Upang suriin ito, kailangan natin ang molekular-statistikong teorya ng mga solusyon. Ang pinakamahirap ay ang pagtukoy ng kapasidad ng init ng mga heterogenous system sa thermodynamic analysis.

Konklusyon
Ang pag-aaral ng kapasidad ng init ay nagbibigay-daan sa iyong kalkulahin ang balanse ng enerhiya ng mga prosesong nagaganap sa mga kemikal na reactor, gayundin sa iba pang mga kagamitan sa paggawa ng kemikal. Bilang karagdagan, ang halagang ito ay kinakailangan para sa pagpili ng pinakamainam na uri ng mga coolant.
Sa kasalukuyan, ang pang-eksperimentong pagpapasiya ng kapasidad ng init ng mga sangkap para sa iba't ibang mga pagitan ng temperatura - mula sa mababang halaga hanggang sa mataas na halaga - ay ang pangunahing opsyon para sa pagtukoy ng mga thermodynamic na katangian ng isang sangkap. Kapag kinakalkula ang entropy at enthalpy ng isang sangkap, ginagamit ang mga integral ng kapasidad ng init. Ang impormasyon tungkol sa kapasidad ng init ng mga kemikal na reagents sa isang tiyak na hanay ng temperatura ay nagbibigay-daan sa iyo upang kalkulahin ang thermal effect ng proseso. Ang impormasyon sa kapasidad ng init ng mga solusyon ay ginagawang posible na kalkulahin ang kanilang mga thermodynamic na parameter sa anumang mga halaga ng temperatura sa loob ng nasuri na pagitan.
Halimbawa, ang isang likido ay nailalarawan sa pamamagitan ng paggasta ng bahagi ng init upang baguhin ang halaga ng potensyal na enerhiyamga molekulang tumutugon. Ang halagang ito ay tinatawag na "configuration" na kapasidad ng init, na ginagamit upang ilarawan ang mga solusyon.
Mahirap magsagawa ng ganap na mga kalkulasyon sa matematika nang hindi isinasaalang-alang ang mga thermodynamic na katangian ng isang substance, ang estado ng pagsasama-sama nito. Iyon ang dahilan kung bakit para sa mga likido, gas, solid, tulad ng isang katangian tulad ng partikular na kapasidad ng init ay ginagamit, na ginagawang posible upang makilala ang mga parameter ng enerhiya ng isang sangkap.






